Идентифицирован фермент мозга, вызывающий никотиновую зависимость и пристрастие к курению
Источник: Medical X Press

Никотиновая зависимость остается одной из самых серьезных проблем общественного здравоохранения во всем мире, вызванной изменениями в мозге, которые усиливают повторяющееся употребление и делают отказ от курения чрезвычайно трудным. На протяжении десятилетий ученые уделяли основное внимание нейронам, чтобы объяснить, как происходят эти изменения. Однако все больше фактов свидетельствует о том, что другие клетки мозга могут играть гораздо более активную роль в формировании зависимого поведения, чем считалось ранее.
Роль астроцитов в никотиновой зависимости
Основываясь на этом изменении в понимании, группа исследователей под руководством профессора Эун Сан Чо из факультета биологических наук Пусанского национального университета, Республика Корея, обнаружила, как астроциты активно способствуют изменениям в мозге, вызванным никотином, раскрыв ранее упускавшийся из виду механизм, связанный с астроцитарной глутаминсинтетазой (GS). GS является важным ферментом для регуляции глутамата, основного возбуждающего нейромедиатора мозга.
Исследование опубликовано в журнале Acta Pharmaceutica Sinica B.
«Большинство исследований никотиновой зависимости традиционно сосредоточено на нейронах, при этом роль глиальных клеток игнорируется. Наше инновационное исследование демонстрирует, что астроциты взаимодействуют с нейронами в системе вознаграждения мозга, регулируя никотинозависимое поведение, что способствует продвижению современного понимания никотиновой зависимости», — говорит проф. Чо.
Основные выводы исследования
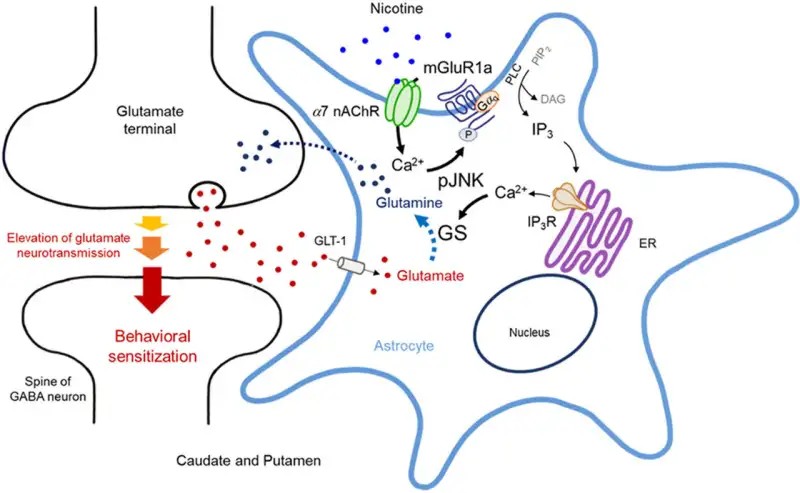
В ходе данного исследования ученые неоднократно вводили крысам никотин и обнаружили, что воздействие никотина стимулировало α7-никотиновые ацетилхолиновые рецепторы на астроцитах хвостатого ядра и путамена головного мозга, вызывая всплеск внутриклеточного кальция.
Этот рост кальция привел к активации фосфорилированной c-Jun N-концевой киназы (pJNK), сигнальной молекулы, которая, как известно, реагирует на клеточный стресс и воздействие лекарственных препаратов.
После активации JNK далее взаимодействовала с метаботропным глутаматным рецептором 1a (mGluR1a), усиливая активность GS и активируя глутамат-глутаминовый путь, что приводило к усилению сенсибилизации двигательной системы.
Для блокирования взаимодействия между pJNK и mGluR1a был использован специально разработанный ингибирующий пептид. При введении этого пептида непосредственно в хвостатое ядро и путамен крыс, подвергавшихся многократному воздействию никотина, обычное увеличение активности GS значительно снижалось.
С точки зрения поведения, это вмешательство ослабляло сенсибилизацию двигательной активности, демонстрируя, что астроцитарная сигнализация является ключевым фактором, вызывающим изменения в мозге под воздействием никотина.
Последствия для будущих исследований в области зависимости
Эти результаты открывают новые направления для исследований в области зависимости, подчеркивая важность коммуникации между нейронами и глией. Хотя никотиновая зависимость широко признана как нарушение глутаматной сигнализации, это исследование показывает, что астроциты участвуют в молекулярных процессах, которые усиливают повторное употребление никотина. Хотя эта работа является доклинической, ее значение для долгосрочных исследований является значительным.
«Хотя клиническое применение этих исследований займет время, а их непосредственное применение на человеке остается неопределенным, эта работа углубляет наше понимание никотиновой зависимости, прокладывая путь для разработки терапевтических стратегий, которые в конечном итоге поддержат усилия по отказу от курения», — заключает профессор Чо.




